Agencja Oceny Technologii Medycznych i Taryfikacji (AOTMiT): jej rola w polskim systemie ochrony zdrowia

Grafika autorstwa Pauliny Smoły
Autorka: Paulina Smoła
Misją Agencji Oceny Technologii Medycznych i Taryfikacji (AOTMiT) jest podnoszenie standardów i jakości ochrony zdrowia w Polsce – usprawnianie procesu podejmowania decyzji dotyczących finansowania świadczeń opieki zdrowotnej. Kluczem do tego jest zasada „medycyny opartej na dowodach naukowych”, w skrócie EBM (ang. Evidence Based Medicine), a jej praktycznym wcieleniem mechanizm oceny technologii medycznych, czyli HTA (ang. Health Technology Assesment) [4]. Ocena technologii medycznych jest kluczowa w mądrym, efektywnym kosztowo dysponowaniu zasobami systemu zdrowotnego (więcej na ten temat przeczytać można w tekście Tomasza Bochenka na Blogu IZP).
AOTMiT powstała już w 2006 roku – oryginalnie jako AOTM (Agencji Oceny Technologii Medycznych). W 2009 roku AOTM uzyskała status państwowej jednostki organizacyjnej posiadającej osobowość prawną, stając się integralną częścią procesu tworzenia koszyków świadczeń gwarantowanych [2]. W 2015 roku jej działalność została poszerzona o pomoc w prawidłowej wycenie świadczeń zdrowotnych dla NFZ („…i Taryfikacji”) i wtedy też przyjęła aktualną nazwę: AOTMiT.
AOTMiT jest instytucją państwową nadzorowaną przez ministra zdrowia (MZ). Wspiera podejmowanie decyzji w systemie opieki zdrowotnej i dostarcza kompleksowych informacji z zakresu oceny technologii medycznych. Angażuje się także w działalność badawczą i rozwojową w kraju i zagranicą. Struktura agencji określona jest statutem, który nadaje i zmienia MZ. Zadania i uprawnienia a także kwestie finansowe i sposób prowadzenia księgowości podlegają odpowiednim regulacjom prawnym. Dwa podstawowe dla agencji akty prawne to:
- Znowelizowana w 2009 roku ustawa z dnia 27 sierpnia 2004 roku o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych (Dz.U. z 2018 roku poz. 1510 z późn. zm.);
- Ustawa z dnia 12 maja 2011 roku o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych (Dz.U. z 2017 roku poz. 1844 z późn. zm.).
W AOTMiT działają dwa organy opiniodawczo-doradcze: Rada Przejrzystości oraz Rada do spraw Taryfikacji. Członkowie rad powoływani są przez MZ na kadencję trwającą sześć lat.
Rada Przejrzystości
Rada Przejrzystości [1] przygotowuje dla MZ stanowisko w sprawie:
- kwalifikacji świadczeń jako gwarantowanych (tj. finansowanych w całości lub w części ze środków publicznych, NFZ [2]);
- zmiany sposobu finansowania świadczeń, technologii medycznych (leków, urządzeń, procedur diagnostycznych i terapeutycznych, a także organizacyjnych systemów wspomagających [5,2]);
- importu docelowego, polegającego na sprowadzaniu z zagranicy produktów leczniczych oraz środków spożywczych specjalnego przeznaczenia żywieniowego nieposiadających pozwolenia na dopuszczenie do obrotu w Polsce, a niezbędnych dla ratowania życia lub zdrowia pacjenta [7];
- usunięcia świadczenia gwarantowanego z koszyka świadczeń gwarantowanych [2];
- zmiany technologii medycznych;
- zasadności objęcia refundacją: leku, środka spożywczego specjalnego przeznaczenia żywieniowego lub wyrobu medycznego.
Rada Przejrzystości wydaje też opinie:
- o projektach programów polityki zdrowotnej (realizowanych przez samorządy terytorialne);
- w sprawie zalecanych technologii medycznych;
- w sprawie działań przeprowadzanych w ramach programów polityki zdrowotnej oraz warunków realizacji tych programów, dotyczących danej choroby lub danego problemu zdrowotnego.
Rada Przejrzystości wykonuje też inne zadania zlecone przez Prezesa AOTMiT.
Rady do spraw Taryfikacji
Do zadań Rady do spraw Taryfikacji należą z kolei zadania takie, jak [1]:
- Opiniowanie planu taryfikacji (stanowi on podstawę działań związanych z określeniem taryfy świadczeń i jest sporządzany na dany rok kalendarzowy) i metodyki taryfikacji świadczeń [10].
- Prowadzenie konsultacji w sprawie taryfy świadczeń.
- Wydawanie stanowisk w sprawie ustalenia taryfy świadczeń.
- Realizacja innych zadań zleconych przez Prezesa AOTMiT.
Rola AOTMiT w ochronie zdrowia w Polsce
Do instytucji dysponujących środkami publicznymi na ochronę zdrowia w Polsce należą MZ i NFZ. MZ pełni funkcję zarówno regulatora, jak i płatnika (częściowo, niektórych świadczeń): finansuje procedury wysokospecjalistyczne lub obligatoryjne szczepienia. Definiuje koszyk świadczeń gwarantowanych – w ramach rozporządzeń ministerialnych – a także wdraża narodowe programy zdrowotne. NFZ z kolei dysponuje składkami zdrowotnymi na świadczenia opieki zdrowotnej. W ramach tego zawiera kontrakty ze świadczeniodawcami na udzielenie tych świadczeń gwarantowanych oraz płaci za nie.
AOTMiT w Polsce pełni funkcję doradczą w ramach oceny technologii medycznych – na potrzeby ustalania koszyka świadczeń gwarantowanych, tworzenia wytycznych klinicznych i programów polityki zdrowotnej oraz taryfikacji świadczeń. Odgrywa kluczową rolę w podejmowaniu decyzji o refundacji świadczeń.
Decyzje o refundacji technologii medycznych w Polsce przebiegają następująco:
- Złożenie wniosku o refundację do MZ (przez np.: firmę farmaceutyczną, konsultanta krajowego).
- MZ zleca AOTMiT opracowanie rekomendacji w sprawie zasadności refundacji.
- Prezes AOTMiT zbiera opinie od konsultantów krajowych i Prezesa NFZ, przekazuje je Radzie Przejrzystości, która na tej podstawie przygotowuje opinię. Na podstawie tej opinii Prezes AOTMiT przygotowuje rekomendację co do zasadności lub niezasadności refundacji i przekazuje ją MZ.
- MZ podejmuje ostateczną decyzję odnośnie tego, czy technologia będzie finansowana ze środków NFZ.
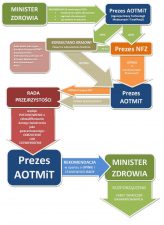
Ryc. 1. Proces tworzenia koszyka świadczeń gwarantowanych z udziałem AOTMiT | Opracowane: M. Zabdyr-Jamróz, tłum. Paulina Smoła
Zadania AOTMiT
Ocena technologii medycznych obejmuje dwa procesy: ocenę analityczną i ocenę wartościującą. Analitycy AOTMiT pracują zgodnie z wytycznymi oceny technologii medycznych (wytycznymi HTA) [7], co zapewnia wysoką jakość. Ocena analityczna jest procesem naukowym, który opiera się na systematycznie zebranych, wiarygodnych, najlepszych dostępnych dowodach naukowych. Składa się z trzech aspektów analizy, odpowiadających na trzy zasadnicze pytania:
- Analiza kliniczna dostarcza informacji, czy dana technologia medyczna przyniesie oczekiwane korzyści zdrowotne w porównaniu z komparatorem (produkt leczniczy lub placebo, stosowanym w badaniu klinicznym, w grupie kontrolnej, jako substancja porównawcza).
- Analiza ekonomiczna wskazuje, czy koszt uzyskania dodatkowej korzyści z zastosowaniem danej technologii jest możliwy do zrealizowania.
- Analiza wpływu na budżet, odpowiadająca na pytanie: „Jak wprowadzenie finansowania danej technologii medycznej wpłynie na budżet płatnika?”.
Ocena wartościująca nie jest zależna od oceny analitycznej. Oprócz dowodów naukowych bierze także pod uwagę: priorytety zdrowotne, skutki następstw choroby, znaczenie dla zdrowia pacjentów, zagadnienia organizacyjne i prawne, oraz kwestie etyczne. Te ostatnie są szczególnie ważne w problematyce leczenia bólu, stosowania leków sierocych (leków wykorzystywanych w leczeniu chorób rzadko występujących), opiece paliatywnej (jest to opieka nad pacjentami chorującymi na nieuleczalne choroby w końcowym okresie życia) [1].
W oparciu o ustawę o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych, do kluczowych zadań AOTMiT należą [2,4]:
- Wydawanie rekomendacji w sprawie kwalifikacji świadczeń do koszyka świadczeń gwarantowanych.
- Wydawanie rekomendacji w sprawie: usunięcia świadczenia z koszyka, zmiany poziomu lub sposobu finansowania lub warunków realizacji świadczenia, zmiany technologii medycznej.
- Wydawanie opinii w sprawie ratunkowego dostępu do technologii lekowej (Ratunkowy Dostęp do Technologii Lekowych stanowi mechanizm finansowania leków w sytuacjach, w których możliwe jest wydłużenie życia pacjenta lub znacząca poprawa jego zdrowia i wykorzystane zostały dostępne refundowane technologie lekowej [6]).
- Wydawanie opinii w sprawie programów polityki zdrowotnej (programy polityki zdrowotnej – programy opracowane, wdrażane, realizowane i finansowane przez jednostki samorządu terytorialnego w przypadku, gdy dotyczą świadczeń gwarantowanych [2]).
- Wydawanie rekomendacji w sprawie zalecanych technologii medycznych, działań przeprowadzonych w ramach programów polityki zdrowotnej oraz warunków realizacji tych programów, dotyczących danej choroby lub danego problemu zdrowotnego.
- Wydawanie rekomendacji w sprawie objęcia refundacją produktu leczniczego lub środka spożywczego specjalnego przeznaczenia żywieniowego.
- Wydawanie rekomendacji w sprawie zasadności wydawania zgody na refundację produktu leczniczego lub środka spożywczego specjalnego przeznaczenia żywieniowego w trybie importu docelowego (import docelowy polega na sprowadzaniu z zagranicy produktów leczniczych oraz środków spożywczych specjalnego przeznaczenia żywieniowego nieposiadających pozwolenia na dopuszczenie do obrotu w Polsce, a niezbędnych dla ratowania życia lub zdrowia pacjenta [7]).
- Wydawanie opinii Rady Przejrzystości w sprawie objęcia refundacją leku we wskazaniu odmiennym, niż określone w Charakterystyce Produktu Leczniczego (tzw. stosowanie „off–label” [9]).
- Inne zlecone zadania (np. wydanie opinii czy tworzenie materiałów analitycznych).
- Określenie taryf świadczeń [2].
Do dodatkowych zadań AOTMiT należą [4]:
- Tworzenie wytycznych metodologicznych.
- Współpraca międzynarodowa.
- Działalność szkoleniowa.
- Udział w pracach legislacyjnych na polu krajowym i międzynarodowym (np. rozporządzenie dotyczące wspólnej oceny klinicznej w UE).
Rola AOTMiT szczególnie widoczna jest na etapie opiniowania i oceny nowych technologii medycznych, które są rozważane pod kątem włączenia ich do koszyka świadczeń gwarantowanych lub usunięcia z tego koszyka.
Objęcie refundacją i ustalenie ceny zbytu leku
W przypadku składania wniosku refundacyjnego wraz z uzasadnieniem, odpowiedzialny za niego podmiot zawiera w nim m.in.: analizę kliniczną, analizę ekonomiczną, analizę wpływu na budżet podmiotu zobowiązanego do finansowania świadczeń ze środków publicznych i analizę racjonalizacyjną (w przypadku, gdy analiza wpływu na budżet podmiotu zobowiązanego do finansowania świadczeń ze środków publicznych przedstawia wzrost kosztów refundacji). Proces objęcia refundacją leków składa się z następujących etapów:
I etap: Przeprowadzenie oceny przekazanych analiz, na podstawie których opracowywana jest analiza weryfikacyjna, następnie przekazywana Radzie Przejrzystości oraz wnioskodawcy. Zamieszczona ona zostaje także w Biuletynie Informacji Publicznej AOTMiT.
II etap: Zaznajomienie się Rady Przejrzystości z analizą weryfikacyjną, a następnie wydanie stanowiska odnoszącego się do zasadności finansowania ze środków publicznych.
III etap: Przygotowanie rekomendacji przez Prezesa AOTMiT, która zgodnie z art. 35 ust. 6. pkt 3 Ustawy z dnia 12 maja 2011 roku o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych zawiera [3]: wskazanie dowodów naukowych, na podstawie których została wydana rekomendacja, wskazanie technologii alternatywnych, omówienie wpływu na wydatki podmiotu zobowiązanego do finansowania świadczeń ze środków publicznych i świadczeniobiorców, wskazanie i omówienie rekomendacji klinicznych oraz refundacyjnych, wskazanie wartości progowej ceny zbytu netto, przy której stosunek kosztów do uzyskiwanych efektów zdrowotnych nie jest większy od progu kosztu uzyskania dodatkowego roku życia skorygowanego o jakość.
IV etap: Wydanie rekomendacji przez Prezesa AOTMiT, która może być zgodna lub nie ze stanowiskiem Rady Przejrzystości.
V etap: Przekazanie przygotowanej rekomendacji do MZ oraz umieszczenie owej rekomendacji w Biuletynie Informacji Publicznej AOTMiT.
Taryfikacja świadczeń opieki zdrowotnej
Zadania AOTMiT związane z taryfikowaniem świadczeń obejmują [1]: ustalanie taryfy świadczeń, opracowywanie propozycji zaleceń dotyczących standardu rachunku kosztów, opracowywanie, weryfikacja, gromadzenie, udostępnianie i upowszechnianie informacji o metodologii oraz zasadach ustalania taryfy świadczeń. Taryfikacja świadczeń opieki zdrowotnej jest prowadzona zgodnie z planem taryfikacji AOTMiT (stanowi on podstawę działań związanych z określeniem taryfy świadczeń i jest sporządzany na dany rok kalendarzowy) [10,11], który został zatwierdzony przez MZ. Projekt planu taryfikacji AOTMiT przekazywany jest do oceny Prezesowi NFZ oraz Radzie do spraw Taryfikacji.
Proces taryfikacji świadczeń opieki zdrowotnej składa się z następujących etapów:
I etap: Sporządzenie raportu przez Prezesa AOTMiT w sprawie ustalenia taryfy świadczeń oraz zwrócenie się do Rady do spraw Taryfikacji o wydanie stanowiska w sprawie ustalenia taryfy świadczeń. Określana jest ona na podstawie dostępnych danych i jest publikowana (po otrzymaniu zatwierdzenia przez MZ) w Biuletynie Informacji Publicznej AOTMiT w formie obwieszczenia.
II etap: Wydanie stanowiska w sprawie ustalenia taryfy świadczeń w terminie 30 dni od dnia otrzymania raportu przez Radę do spraw Taryfikacji. Stanowisko wydawane jest na podstawie raportu, jak również ustaleń podjętych w trakcie konsultacji w sprawie taryfy. Konsultacja może odbywać się z: konsultantem krajowym w dziedzinie medycyny związanej ze świadczeniem opieki zdrowotnej podlegającym taryfikacji; przedstawicielami ogólnopolskich towarzystw naukowych w dziedzinie medycyny związanej ze świadczeniem opieki zdrowotnej podlegającym taryfikacji; przedstawicielami organizacji społecznych działających na rzecz praw pacjentów; przedstawicielami organizacji świadczeniodawców oraz innymi podmiotami lub osobami [1].
III etap: Przesłanie projektu przez Prezesa AOTMiT, zawierającego określenie taryfy świadczeń oraz raport w sprawie ustalenia taryfy świadczeń, do MZ.
IV etap: Wydanie decyzji MZ, po zapoznaniu się z otrzymanymi dokumentami. Decyzja ta zatwierdza bądź w szczególnych przypadkach zmienia taryfę świadczeń, określoną przez Prezesa AOTMiT.
V etap: Przekazanie przez MZ danej taryfy świadczeń do Prezesa AOTMiT w celu opublikowania (w formie obwieszczenia) w Biuletynie Informacji Publicznej AOTMiT.
Podsumowanie
Zapewnianie społeczeństwu dostępu do diagnostyki, leczenia, rehabilitacji i promocji zdrowia, powinno spełniać wymogi skuteczności i bezpieczeństwa. Kluczowe jest zarządzanie zasobami w opiece zdrowotnej i całej ochronie zdrowia w sposób najbardziej efektywny kosztowo. Agencja Oceny Technologii Medycznych i Taryfikacji istnieje po to, by do tego celu dążyć. W tym wymiarze AOTMiT wpływa na zawartość koszyka świadczeń poprzez ocenę nowych technologii medycznych. Przed podjęciem decyzji o refundacji MZ bierze pod uwagę zalecenia i opinie Prezesa AOTMiT, Rady Przejrzystości, a także Rady do spraw Taryfikacji. Dzięki funkcjonowaniu Agencji w systemie ochrony zdrowia w Polsce, zarówno skuteczność jak i wysoki standard jakości opieki zdrowotnej, stają się możliwe do osiągnięcia. Ze względu na swój profil AOTMiT może stanowić miejsce pracy absolwentów kierunków realizowanych w Instytucie Zdrowia Publicznego WNZ UJ CM w Krakowie.
Autorka: Paulina Smoła
Studentka 3. roku kierunku studiów Organizacja i Ekonomika Ochrony Zdrowia
Konsultacja merytoryczna: Tomasz Bochenek
Blog Zdrowia Publicznego, red. M. Zabdyr-Jamróz, Instytut Zdrowia Publicznego UJ CM, Kraków: 14 maja 2021
Źródła
- Lipińska A., Nawrocki T., Patyna M., Płusa A., Pomorski M., Ziębińska A.: Miejsce i znaczenie AOTMiT w polskim systemie ochrony zdrowia. Zdrowie Publiczne i Zarządzanie., 2019; 17(4):183-193.
- Ustawa z dnia 27 sierpnia 2004 roku o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych (Dz.U. z 2018 roku poz. 1510 z późn. zm.).
- Ustawa z dnia 12 maja 2011 roku o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych (Dz.U. z 2017 roku poz. 1844 z późn. zm.).
- Opracowania i dokumenty własne. Strona internetowa: Agencji Oceny Technologii Medycznych i Taryfikacji: AOTMiT [dostęp online 3 marca 2021]. Adres: https://www.aotm.gov.pl/.
- Opiniowane technologie medyczne. Strona internetowa Agencji Oceny Technologii Medycznych i Taryfikacji: AOTMiT [dostęp online 10 marca 2021]. Adres: https://www.aotm.gov.pl/informacje-dla-przemyslu/opiniowane-technologie-medyczne/.
- RDTL. Strona internetowa Agencji Oceny Technologii Medycznych i Taryfikacji. AOTMiT [dostęp online 10 marca 2021]. Adres: https://www.aotm.gov.pl/produkty-lecznicze/rdtl/.
- Import docelowy. Strona internetowa Narodowego Funduszu Zdrowia: NFZ [dostęp online 10 marca 2021]. Adres: http://www.nfz-warszawa.pl/dla-swiadczeniodawcow/recepty-leki-apteki/informacje-ogolne/import-docelowy/.
- Wytyczne Oceny Technologii medycznych (HTA, ang. health technology assessment). Agencja Oceny Technologii Medycznych i Taryfikacji. Warszawa. 2018. [dostęp online 10 marca 2021]. Adres: https://www.aotm.gov.pl/media/2020/07/20160913_Wytyczne_AOTMiT.pdf.
- Off-label, czyli pozarejestracyjne stosowanie leku. Strona internetowa: OPIEKA.FARM Medyczne wsparcie w codziennej pracy. [dostęp online 10 marca 2021]. Adres: https://opieka.farm/recepty/off-label-czyli-pozarejestracyjne-stosowanie-leku/.
- Plan Taryfikacji na 2021. Strona internetowa Agencji Oceny Technologii Medycznych i Taryfikacji: AOTMiT [dostęp online 10 marca 2021]. Adres https://www.aotm.gov.pl/media/2020/08/Plan-Taryfikacji-na-2021-rok_Minister-Zdrowia_zalacznik.pdf.
- Taryfikacja. Strona internetowa Agencji Oceny Technologii Medycznych i Taryfikacji: AOTMiT [dostęp online 10 marca 2021]. Adres: https://www.aotm.gov.pl/taryfikacja/.
 FACEBOOK
FACEBOOK INSTAGRAM
INSTAGRAM X
X LINKEDIN
LINKEDIN YOUTUBE
YOUTUBE